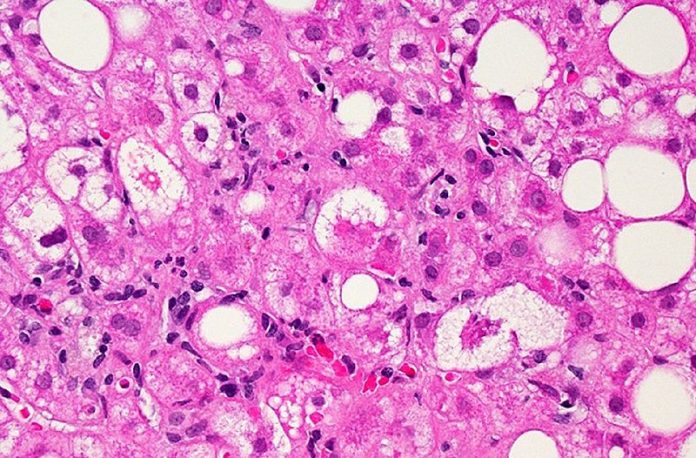
A Rezdiffra-t (resmetirom) az Egyesült Államok FDA jóváhagyta nem cirrhoticus, nem alkoholos steatohepatitisben (NASH) szenvedő felnőttek kezelésére, amelyek mérsékelt vagy előrehaladott májhegesedéssel (fibrózissal) járnak, diétával és testmozgással együtt.
Eddig a nem cirrhoticus, nem alkoholos steatohepatitisben (NASH) szenvedő betegeknek, akiknél jelentős májhegesedés is volt, nem volt olyan gyógyszer, amely közvetlenül kezelhette volna májkárosodás. FDA-k A Rezdiffra jóváhagyása első alkalommal biztosít kezelési lehetőséget ezeknek a betegeknek a diéta és a testmozgás mellett.
A NASH az alkoholmentes zsírok progressziójának eredménye máj betegség ahol máj a gyulladás idővel májhegesedéshez és májműködési zavarokhoz vezethet. A NASH gyakran társul más egészségügyi problémákkal is, mint például a magas vérnyomás és a 2-es típusú cukorbetegség. Legalábbis egy becslés szerint az Egyesült Államokban körülbelül 6-8 millió ember szenved NASH-ban, közepes vagy előrehaladott májhegességgel, és ez a szám várhatóan növekedni fog.
A Rezdiffra egy pajzsmirigyhormon-receptor részleges aktivátora; ennek a receptornak a Rezdiffra általi aktiválása a májban csökkenti a májzsír felhalmozódását.
A Rezdiffra biztonságossága és hatékonysága
A Rezdiffra biztonságosságát és hatásosságát egy helyettesítő végpont 12. hónapjában végzett elemzése alapján értékelték egy 54 hónapos, randomizált, kettős vak, placebo-kontrollos vizsgálatban. A helyettesítő végpont mértékét mérte máj gyulladás és hegesedés. A megbízónak a jóváhagyás utáni vizsgálatot kell végeznie a Rezdiffra klinikai előnyeinek igazolására és leírására, amelyet ugyanazon 54 hónapos vizsgálat elvégzésével kell elvégezni, amely még folyamatban van. A vizsgálatban való részvételhez a betegeknek rendelkezniük kellett a máj mérsékelt vagy előrehaladott NASH okozta gyulladást mutató biopszia máj hegesedés. A vizsgálatban 888 személyt véletlenszerűen osztottak be a következők valamelyikére: placebo (294 alany); 80 milligramm Rezdiffra (298 alany); vagy 100 milligramm Rezdiffra (296 alany); naponta egyszer, a szokásos NASH-kezelés mellett, amely magában foglalja az egészséges táplálkozással és testmozgással kapcsolatos tanácsadást.
A 12 hónapos májbiopsziák azt mutatták, hogy a Rezdiffra-val kezelt alanyok nagyobb hányada érte el a NASH feloldását vagy a májhegesedés javulását, mint azok, akik placebót kaptak. A 26 milligramm Rezdiffra-t kapó alanyok összesen 27-80%-a, és a 24 milligramm Rezdiffra-t kapó alanyok 36-100%-a tapasztalt NASH feloldódást, és nem romlott a májhegesedés, szemben azoknál, akiknél ez az arány 9-13%. placebót és tanácsot kapott a diétával és a testmozgással kapcsolatban. A válaszok köre a különböző patológusok olvasatait tükrözi. Ezenkívül a 23 milligramm Rezdiffra-t kapó alanyok összesen 80%-a, és a 24 milligramm Rezdiffra-t kapó alanyok 28-100%-a tapasztalt javulást máj scarring and no worsening of NASH, compared to 13% to 15% of those who received placebo, depending on each pathologist’s readings. Demonstration of these changes in a proportion of patients after just one year of treatment is notable, as the betegség typically progresses slowly with most patients taking years or even decades to show progression.
A Rezdiffra mellékhatásai
A Rezdiffra leggyakoribb mellékhatásai a hasmenés és a hányinger voltak. A Rezdiffra bizonyos figyelmeztetéseket és óvintézkedéseket tartalmaz, mint például a gyógyszer okozta májtoxicitás és az epehólyaggal kapcsolatos mellékhatások.
A Rezdiffra alkalmazása kerülendő dekompenzált cirrhosisban szenvedő betegeknél. A betegeknek abba kell hagyniuk a Rezdiffra alkalmazását, ha rosszabbodás jelei vagy tünetei jelentkeznek máj funkciója a Rezdiffra-kezelés alatt.
A Rezdiffra gyógyszerkölcsönhatásai
A Rezdiffra bizonyos más gyógyszerekkel, különösen a koleszterinszint-csökkentő sztatinokkal egyidejű alkalmazása potenciálisan jelentős gyógyszerkölcsönhatásokat eredményezhet. Az egészségügyi szolgáltatóknak a Rezdiffrával való potenciálisan jelentős gyógyszerkölcsönhatásokról, az ajánlott adagolásról és az adagolás módosításáról további információkért olvassák el a teljes felírási információkat.
A FDA jóváhagyta a Rezdiffra-t a gyorsított jóváhagyási útvonalon, amely lehetővé teszi a súlyos állapotok kezelésére szolgáló és kielégítetlen orvosi szükségletet kielégítő gyógyszerek korábbi jóváhagyását olyan helyettesítő vagy köztes klinikai végpont alapján, amely ésszerűen valószínű, hogy előre jelezheti a klinikai előnyöket. A fent említett szükséges, 54 hónapos vizsgálat, amely folyamatban van, a klinikai előnyt 54 hónapos Rezdiffra-kezelés után értékeli.
Rezdiffra áttörést jelentő terápia, Fast Track és Priority Review minősítést kapott erre az indikációra.
A FDA megadta a Rezdiffra jóváhagyását a Madrigal Pharmaceuticalsnak.
***
Forrás:
FDA 2024. Sajtóközlemény – Az FDA jóváhagyja a zsírmájbetegség miatti májhegesedésben szenvedő betegek első kezelését. Feladás dátuma: 14. március 2024. Elérhető: https://www.fda.gov/news-events/press-announcements/fda-approves-first-treatment-patients-liver-scarring-due-fatty-liver-disease
***